岩石から生まれたガラス
第六回は、原子番号14「ケイ素」のお話です。
ケイ素 Siは、この世界にとてもたくさんあります。地球全体では鉄(Fe)、酸素(O)に次いで3番目に多い元素です。特に地表付近の岩石に多く含まれていて、地球表面下約16 kmまでに限ると、質量にして25.8%をケイ素が占めています。これは酸素の49.5%に次ぐ多さです。さらに視野を広げて、宇宙全体を見ても7番目に多い元素とされています。こんなにたくさんあるのに、意外にも生き物の体や生存のためにはあまり使われていません。それで“無機物の主役”といわれることがあるのです。
生物があまり使っていないとしても、こんなにたくさんあるのですから何か使い道はないものでしょうか。単体のケイ素は不安定なため、岩石中では酸素と結合した二酸化ケイ素(SiO2)として存在しています。SiO2といえば、そう、ガラスの主成分ではありませんか!!大量に存在するケイ素という資源を、人類はしっかり使っています。
ガラスは今から約5000年前のメソポタミアで発見されました。あまりに古いことなので言い伝えでしかありませんが、ソーダ灰(炭酸ナトリウム)を売っていた商人が、昼食をつくるためにソーダ灰の入った袋をカマドがわりに使ったところ、ソーダ灰と砂が混ざり、それが熱で融けて透明な液体が流れ出てきて、冷えると半透明の石のようなものになったというのです。こんな偶然によってガラスが発見されたのも、SiO2が砂に含まれているからです。
ガラスは透明で硬くて、化学薬品や様々な環境に対して安定という優れた性質から、食器や窓ガラス、蛍光灯、ビーカーや試験管などの化学実験器具のほか、テレビや太陽光発電パネルの表面の保護など、私たちの生活のいたるところに使われています(写真1)。
また、化工法や添加物を変えることによって、光を曲げる性質をコントロールできるので、眼鏡や顕微鏡、望遠鏡のレンズや、光を使って情報を送る光ファイバーの素材としても使われています。
日本の天文チームが中心になって、超大型望遠鏡をつくろうという国際プロジェクトがハワイで進んでいます。この超大型望遠鏡TMTでは、レンズの代わりに反射鏡で光を集める方式が取られています。反射鏡は492枚の鏡をつなぎ合せてつくられ、全体では口径30mにもなります。この巨大鏡が、気温の変化によって膨張収縮を起こしたら、天体観測に影響が出てしまいます。そうならないために鏡の素材には、低膨張ガラスという特殊ガラスが採用されました。このガラスに金属膜をコーティングして鏡にしたのです。
食器のような身近なものから、最先端の望遠鏡や光ファイバーまで、ガラスの活躍の場は実に広範囲です。改めてすごい素材だと感じます。ただ一点、ガラスの短所を挙げるとすれば、それは割れてしまうことでしょうか。その点は用途によって様々な防止策が図られていて、例えば窓ガラスの場合は割れにくくするだけでなく、割れても破片が飛び散らないように、表面にフイルムが貼られていたりします。

(写真1)ガラス製食器とガラス製レンズを使った望遠鏡(提供:depositphotos)
そもそもガラスって何?
ガラスの扱いやすさは、温度を上げて融かして様々な形がつくれるところです。固まってから研磨して、精密な形をつくることもできます。ガラスは硬いですが、いわゆる固体ではありません。では液体なのか?というと、そうでもありません。気体でないことは明らかです。ガラスは、液体の無秩序な原子配列をもったまま固まった「非結晶固体」なのです。
物質には気体、液体、固体の三つの状態があり、それを「物質の三態」と言います(図1)。物質の三態を、原子や分子などの粒子が見える目で観察できたとすると、固体は粒子がきちんと整列していますが、液体では少し緩んで流動的になっているでしょう。さらに気体では粒子が互いの束縛から解放されて飛び回っています。
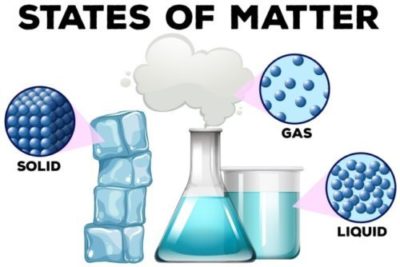
(図1)物質の三態と粒子の様子(提供:depositphotos)
では、ガラスの、“液体の無秩序な原子配列をもったまま固まった状態”とは、どういうことでしょうか。通常、液体が固体になるときには、温度が下がるのに伴って、流動的だった粒子はきちっと整列します。ところがガラスの場合は温度が下がると、ほかの液体よりもドロドロになるため、粒子がきちっと整列する前に、動けなくなってしまうのです(図2)。
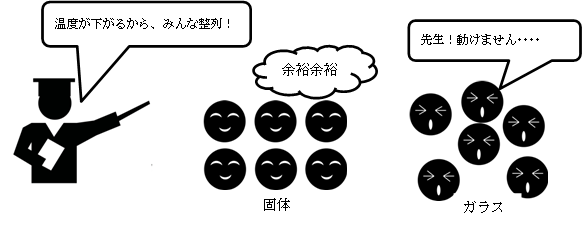 (図2)固体とガラスの違い(イメージ)
(図2)固体とガラスの違い(イメージ)
正確には、このような状態のものをガラスと呼ぶので、ガラスは必ずしもSiO2でできている必要はありません。二酸化ゲルマニウム(GeO2)や五酸化二リン(P2O5)、三酸化二ホウ素(B2O3)などもガラスになります。しかしこれらは耐水性が低かったり、毒性が強かったり、高価であったりといった理由から単独で工業製品になることはありません。そのため、日常生活で“ガラス”といったらSiO2を主成分とするものと考えていいのです。
ところでガラスをつくる際には、SiO2に炭酸ナトリウム(Na2CO3)や炭酸カルシウム(CaCO3)などを加えます。ガラスが発見された時にも、ソーダ灰つまり炭酸ナトリウムが関わっていました。こうした添加物が必要なのは、SiO2の融ける温度を下げて加工しやすくするためと、耐久性を上げるためです。例えば、SiO2にNa2CO3を加えると融ける温度が下がります。ところが、これでガラスをつくると、空気中の水分や二酸化炭素を吸収して2~3日すると、白い粉になってしまうのだそうです。そうならないために、炭酸カルシウムを加え耐久性をもたせます。
ガラスは地球にたくさんあるSiO2を主成分にしていますが、用途によって、安定であったり、割れにくかったり、より透明であったり、光の屈折率が高かったり、膨張しにくかったりと要求されることが変わってきます。それに応えるガラスをつくるのに高い技術があることも覚えておきたいものです。
ケイ素は半導体の代表物質
そして、単体のケイ素は不安定で自然界には存在しないのですが、実は、生活の電化が進んだ現代社会で、単体のケイ素は欠かせないものになっています。「ケイ素とはシリコンのこと」と聞いたらピンとくる人もいると思いますが、単体のケイ素はエレクトロニクスを支える半導体の代表的な材料なのです。
半導体とは、その物質の電気的な性質について言う言葉です。銅のように電気をよく通す物質は“導体”、一方、電気を通さないものは“不導体”と言われます。半導体とは、導体と不導体の中間の電気的な性質をもつ物質です。半導体のこの電気的な性質を利用して、電圧の増幅機能や電気のスイッチング機能を果たす電子デバイスをつくりあらゆる電気製品に埋め込まれています。
ケイ素を電子デバイスに使うには、99.999999999%という超高純度が求められます。11個9が並ぶので、俗にイレブンナインと言われます(写真2)。ケイ素元素は地球上に大量に存在するので、資源の枯渇の心配はありません。ただ、地球上に存在するのはSiO2です。半導体として使える高純度のケイ素を得るには、SiO2を還元しなくてはならず、大量の電力が必要です。そのため高純度の単体ケイ素は、電気料金の安い国でつくられています。

(写真2)純度99.999999999%以上のシリコンインゴットとそれを厚さ1mm程度にスライスしてできたウェーハ(左)。半導体集積回路(右)。ケイ素の単体には金属光沢がある。ウェーハの上に印刷・撮影技術を使って電子回路を書き込み、さまざまな電子デバイスをつくる。一枚のウェーハに書き込む電子回路の数を増やしていくことを集積化といい、集積化によってデバイスの小型化と高性能化が進んできた。半導体集積回路は電子デバイスの一例。この中に、電子回路が書き込まれたウェーハの欠片が入っている。(提供:depositphotos)
さて、今回はケイ素が無機物の主役だということに、納得していただけたでしょうか。そして、「こんなにたくさんあるケイ素を無機物としてしか使わないのはもったいない」と思ったのかどうかはわかりませんが、ケイ素を人工的に有機物にして利用する試みが行われています。すでに便利なものが生まれていますので、それについては次の第七回の「無機物の主役 ケイ素元素(Si)の有機物への挑戦」でご紹介したいと思います。
参考資料:
『トコトンやさしいガラスの本』日刊工業新聞社、2004
『ガラスの科学』日刊工業新聞社、2013
『トコトンやさしい半導体の本』日刊工業新聞社、2009
Canon:http://web.canon.jp/technology/kids/mystery/m_02_07.html
KEYENCE:https://www.keyence.co.jp/ss/products/vision/visionbasics/basic/history/lens.jsp
HITACHI:https://www.hitachi-hightech.com/jp/products/device/semiconductor/ic.html
池田亜希子
最新記事 by 池田亜希子 (全て見る)
- 人間がつくった元素たちは、生活の中にあるの? - 2019年11月18日
- 周期表にない!? 最近、問題のトリチウムって何?(T、原子番号1) - 2019年10月14日
- 柔らかくて使いやすい、この金属にはご用心 鉛(Pb、原子番号82) - 2019年9月16日
