元素記号Ni、原子番号28の元素、ニッケル。世界で生産されるニッケルの約65%がステンレス鋼の製造に、約20%はその他のスチールや非鉄合金に用いられている。高度な建築、輸送、海洋、消費財、航空宇宙、軍事など他方面に使用されていて、我々にとって不可欠な元素である。図1はステンレスで作られた建築物の例、図2はテンレスで作られた歴史ある歩道橋である。

図1 オーステナイト系ステンレス鋼SUS316Lで作られたゴベット・ブリュースター美術館のレン・ライセンター(ニュージーランド、ニュープリマス)
Schwede66 ”Len Lye Centre in November 2018” CC BY-SA 4.0 (WIKIMEDIA COMMONS)

図2 北アイルランドで再建されたAn Gobain(316Lステンレス鋼の歩道橋、もともとは1902年に開通)
Paravel “Replacement Tubular Bridge at the Gobbins Path, Islandmagee, Co. Antrim. The path was refurbished in 2014-15.“CC BY-SA 3.0

EastAntrimMan“New bridge and old bridge remains at The Gobbins“CC BY-SA 4.0
元素の名前がコインのあだ名になっているアメリカの5セント硬貨。その組成は日本の50円および100円硬貨と全く同じ、Cu 75%、Ni 25%。ただし日本の500円硬貨はCu 72%、Ni 20%、Zn 8%なのでニッケルの割合が若干低い。

図3 五十円硬貨、百円硬貨、五百円硬貨(日本)と5セント硬貨(米国)
銅とニッケルとの合金は「白銅」と呼ばれ、ニッケルが含まれることでその合金はきわめて耐摩耗性が高くなり、また長い間、輝きを失うことがない。近年ではニッケルめっきのスチール硬貨も増えており、例えば王立カナダ造幣局の25セント硬貨は、スチールに銅とニッケルをめっきする新しいスタイルの多層構造で組成は94%がスチール、3.8%が銅、2.2%がニッケル。
この組成でまず無印の硬貨が製造される。その後表面に圧印して、はっきりとした硬貨デザインがつけられる。ニッケルには可鍛性があり、数十年の使用が可能な強靭性もある。しかもスチールの中に電磁署名を付けることができるため、例えば自動販売機で偽造硬貨の使用を排除できる。
ニッケルを含まない携帯電話やスマホはない。それくらい現在のエレクトロニクスはニッケルに依存している。リチウムイオン電池のアノード、電磁干渉シールドの塗料、マイクや回路基板、SIMカードにおける酸化防止のめっき、などなどスマホ内の11種類ほどのパーツでニッケルが不可欠な状況にある。
ニッケルは地球上の未来においても豊富な資源と考えられている。十分採掘されつつも100%リサイクル可能な金属であり、まだ十分今後の採掘も可能と考えられている。
実験1 ニッケル水溶液の実験

① 硝酸ニッケル(II)水溶液(緑色)
② ①に水酸化ナトリウム水溶液(6 mol/L)1滴を加えると、淡緑色の水酸化ニッケルが沈殿する。
Ni2++2OH–→ Ni(OH)2↓
③ ①にアンモニア水を滴下すると、淡緑色の水酸化ニッケルが沈殿する。
④ アンモニア水を過剰に加えると青紫色の錯体を生成し、沈殿は溶解する。
Ni2+2NH3+2H2O→Ni(OH)2↓+2NH4+
Ni(OH)2↓+ 6NH3 → [Ni(NH3)6]2+ + 2OH–
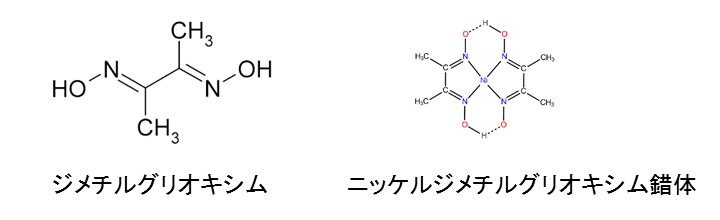
⑤ ①に1%ジメチルグリオキシム溶液を1滴加えると赤色沈殿を生じる。
Ni2++2C4H8O2N2→Ni(C4H7O2N2)2↓+2H+
実験2 ニッケルを含んだケミカルガーデン(化学の花園)
ケミカルガーデンとは写真のように、水ガラス(ケイ酸ナトリウムNa2SiO3水溶液)に固体の金属塩を入れることで成長する樹状のものをいう。
例えば水ガラスとして、ケイ酸ナトリウム(または溶液)を水に溶かして均一になったものを準備する。目安は比重が1.10ぐらいとなるのがよい。ケイ酸ナトリウムは加水分解によってケイ酸のゲル(シリカゲル)となる。2Lのペットボトルに、調整した水ガラスを下から3分の1ほどいれる。次にその中に各金属塩を小さじ半杯程度入れる(量は好み)。使用できる結晶の例として次のようなものがある。
硫酸ニッケル(II)(緑)、硫酸アルミニウム(白)、硫酸銅(II)(青)、塩化クロム(III)(緑)、硫酸鉄(II)(オレンジ色)、塩化コバルト(II)(紫)

ケミカルガーデンの成長の様子
写真・情報提供:千葉大学工学部共生応用化学科佐藤研究室(現 愛媛大学高橋亮治教授による当時の実演記録)
樹状になるのは、ミクロなレベルの中和反応と浸透圧現象によって説明される。金属塩は水に溶解すると、金属イオンの水和錯体中の配位した水分子が一部電離するため弱酸性になる。金属塩が弱酸性であるのに対し、水ガラスは強塩基であるため投入された金属塩表面で局所的な中和反応が生じ、金属塩の表面にケイ酸塩由来のシリカゲルの被膜が形成される。シリカゲルにはたくさんの細孔があり、その膜は半透膜の機能を持つため、内部に水分子が入り込む。
水圧はペットボトルの底ほど大きいまたは低密度の内部溶液は浮力により上昇するため、細長い形が成長する。ただし、その水圧によって先端部分の膜が破れ、またシリカゲル被膜が形成され水分子が入りこむ。この繰り返しによって成長する。成長の速度は水ガラスの濃度や金属塩の種類によって異なるが、数分から1時間程度で成長を観察することができる。
参考文献:
「現在製造している貨幣」独立行政法人 造幣局:https://www.mint.go.jp/operations/production/operations_coin_presently-minted.html
“Coin Specifications”, United States Mint:
https://www.usmint.gov/learn/coin-and-medal-programs/coin-specifications
ニッケル誌「硬貨の進化」、第30号第3巻(2015年)ニッケル協会 東京事務所:
http://www.nickel-japan.com/magazine/pdf/201512_EN.pdf
信州大学 理学部 化学科、ニッケル:
http://zen.shinshu-u.ac.jp/modules/0027005002/
片岡弘、「渦を巻く沈殿反応―ケミカルガーデンとリーゼガング現象―」化学と教育、p.282-283、65巻6号(2017 年)
「ケミカル・ガーデン」、千葉大学 工学部 共生応用化学科 資源反応工学研究室(佐藤智司研究室):http://chem.tf.chiba-u.jp/gacb14/cg.html
山﨑 友紀
最新記事 by 山﨑 友紀 (全て見る)
- 実験講座 番外編 アメリカ、サンフランシスコ湾での天然塩づくり - 2024年3月25日
- 実験講座 番外編 アメリカ カリフォルニアで見た多様な鳥たち - 2024年1月29日
- 実験講座 番外編 アメリカCalifornia Academy of Science(科学博物館)訪問 - 2023年11月27日