元素記号P、原子番号15番の元素、リン。
金でないものを金に変えようという錬金術が化学の発展に貢献したことは間違いない。ドイツの錬金術師ヘンニヒ・ブラントがルネサンスの時代1669年にヒト(おそらく本人)の尿から単離に成功したとされている。ブラントは尿を集めては空気遮断下で蒸発し続けた結果、容器に光る物質(黄リンと考えられる)を得ることができた。本人はこれが錬金術に欠かせない「賢者の石」だと思った、という逸話がある。

左から黄リン(または白リン)、赤リン、黒リン
出典:WIKIMEDIA COMMONS
(左)BXXXDによる”White phosphorus under water”ライセンスはCC BY-SA 3.0
(中)Tomihahndorfによる”Red phosphor”ライセンスはPD
(右)Alshaer666による”Crystals of Black Phosphorus in sealed ampoule”ライセンスはCC BY-SA 3.0
リンには、黄(純粋なものは白)、赤、紫、黒の色の名前がそれぞれつけられた同素体が4つある。そして、人類のリンの利用は化学肥料の発端にさかのぼる。リンの原料のほとんどが天然のリン鉱石であるが、一部欧州や日本などで下水汚泥等からのリンがリサイクルされている。リンの用途は多岐にわたり、マッチ、洗剤、食品添加物、歯磨き材、電池材料(特にリチウムイオン電池)、農薬、医薬品、化学兵器などがある。猛毒サリンもリンの化合物である。研究者らの見解によると、世界人口の増加と農業の拡大に伴うリン化学肥料の生産と消費がこのまま続けば、リン資源はあと数10年で枯渇すると見積もられており、リンの有効利用やリサイクルが今後さらに重要視されるだろう。
墓場で出るといわれる「火の玉」も動物やヒトの死体由来のリン光であると考えられている。リンは生物に欠かせない重要な元素であり肥料の三大元素、窒素N、リンP、カリウムKの一つでもある。リンは動物の骨や歯の骨格(水酸燐灰石またはヒドロキシアパタイトCa5(PO4)3(OH))、頭髪や皮膚に含まれており、分子レベルで見るとDNA、ATPなどを形成する元素である。
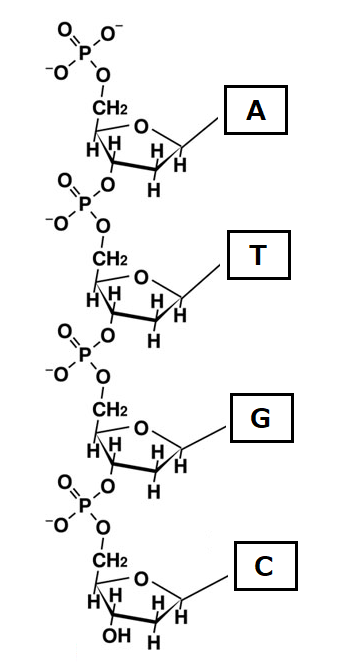
DNAのリン酸エステル結合の一部
(A、T、G、Cは塩基のアデニン、チミン、グアニン、シトシンの略)
実験1 リンの発光実験
黄リンは猛毒で危険性があるため、入手が極めて困難である。現在日本では黄リンは製造されていない。黄リンの自然発火やリン光現象を学校などで実験的に演示するのが困難であるが、最近ではインターネット上の例えば理科ねっとわーくなどでその映像が公開されている。
一方、赤リンが入手できれば、赤リンの相転移で生じた黄リンを自然発火させて観察する方法もある。この実験では、加熱作業時に発生する白煙を吸引しないように注意する。
手順:試験管に赤リンを数グラム程度入れ、下からガスバーナーで加熱していく。若干振り交ぜながら加熱するだけで、赤リンの燃焼と、黄リンに相転移した部分の黄リンの自然発光の両方を観察することができる。試験管に二酸化炭素を供給すると黄リンへの相転移をスムーズにできる。空気(酸素)の供給により、黄リンの発光に勢いがつく。

赤リンを加熱する様子(左)、黄リンの発光と赤リンの燃焼が混在した状態(右)
リンの乾留・黄燐の発光(下)
(提供:公立大学法人 都留文科大学教養学部学校教育学科山田暢司特任教授)
実験2 キャベツ中のリンを検出してみよう
リン酸とモリブデン酸アンモニウムとを酸性下で反応させると、リンモリブデン酸錯体が生じる。これを還元すると青色のモリブデンブルーが得られるので、これの波長と吸光度からリンの量を求めることができる。この方法はモリブデンブルー法として、食品分析や環境分析に汎用されている。
ちなみにリンは多種多様な食品に含まれていることから不足よりも摂取過多に注意する必要があるとされ、過剰摂取はカルシウムの吸収が抑制されるとされている。リン摂取の目安量としては、成人男子が1日あたり1000mg、成人女子が 800mgである。リンを多く含む食品としては清涼飲料水、魚類、乳製品、肉類などがあげられる。野菜中のリンは煮だすことによって10%ほど除去できること、塩ゆでが除去に効果があることがわかっている。キャベツの場合100gあたり約27mgのリンが含まれるとされている。以下のような実験では煮出す温度と時間によるが、キャベツ100 gから7 mg程度の溶出したリンを検出することができる。
手順:
1)キャベツを千切りにして試験管に入れやすい大きさにする。キャベツ3 gと純水7 gを試験管に一緒に入れ、キャベツが水に浸るようにする。
2)沸騰湯浴でキャベツの入った試験管を一定時間(例えば10分)浸して煮出す。また、温度や時間を変えて実験すると、リンの溶出量の温度、時間依存性を求めることができる。
3)リンの標準溶液として、リン酸二水素カリウムKH2PO4を純水に溶かして調製する。リンP換算で0~200 ppmの濃度(例えば0、50、100、150、200 ppmなど)の複数の標準溶液を準備する。
4)モリブデン酸アンモニウム溶液を調整する。(NH4)6Mo7O24・4H2O 50gを600mLの水に溶かし、濃硫酸150 mLを水300 mLに溶かして放冷したものと丁寧に混ぜる。
5)よく洗浄された50 mLのメスフラスコを標準溶液および試料溶液の数だけ準備する。キャベツを煮出した試験管の各試料溶液5 mL、および準備した各濃度の標準溶液5 mLをそれぞれ50 mLのメスフラスコに正確に入れる。
6)各メスフラスコにモリブデン酸アンモニウム溶液4 mLずつを加えて混和し、2~3分間放置する。
7)それぞれのフラスコに別途準備しておいた0.5%ヒドロキノン溶液(還元剤)4 mL、10%亜硫酸ナトリウム4 mLをさらに順に加え、最終的に純水で50 mLまでメスアップしてよく混和して20分放置する。ヒドロキノンの代わりに還元剤として1%アミドール(2,4-ジアミノフェノールニ塩酸塩)水溶液を用いてもよい。
8)紫外可視吸光光度計の測定波長を880 nm(740 nmも可)に設定し、各試料の吸光度を測定する。3)で調製した各濃度の標準溶液の吸光度と濃度の関係を検量線にして、未知濃度のサンプル中のリン濃度を決定する。

(左上)リン酸標準溶液の呈色の様子 (上中央)千切りされたキャベツ (右上)試験管に試料を入れている様子
(左下)試料を沸騰湯浴で加熱している様子 (下中央)キャベツから溶出したリンを含む溶液が呈色している様子 (右下)実試料および標準溶液を分光光度計で測定している様子
(写真提供:名古屋栄養専門学校)
参考文献:
桜井弘「元素111の新知識(ブルーバックス)」、講談社、1997年
サイエンスチャンネル、elements~メンデレーエフの奇妙な棚~(2)光をもたらすもの~錬金術と元素~:http://sciencechannel.jst.go.jp/C043302/
“迫り来るリン資源の危機”、日経サイエンス、 2009年9月号
岩藤英司、“赤リン、 黄リンの簡単な演示法~赤リンから相転移した黄リンの利用~”、化学と教育、2006年54巻1号p.26-27
松永剛一・佐藤英俊、“リンの工業利用”、生物工学、第90巻2012年 、第8号p.477-480:http://www.sbj.or.jp/wp-content/uploads/file/sbj/9008/9008_tokushu_4.pdf
実施困難な実験・観察集3 リンを用いた実験とその性質:
https://rika-net.com/contents/cp0490b/contents/cheindex1.html
中村道徳、“リン酸の比色定量法 I.”、化学と生物、Vol. 3, No. 1、p.39-46、1965年
中村道徳、“リン酸の比色定量法 II.”、化学と生物、Vol. 3, No. 2、p.91-98、1965年
松本和子・酒井健、“モリブデン・ブルーの発色とリン定量への応用(化学への招待)”、化学と教育、1987 年 35 巻 5 号 p. 420-423
「ゆで」「炊き」「水煮」によるカリウム・リンの除去率:https://www.mealtime.jp/mealtime_shop/pdf/look03.pdf
厚生労働省「日本人の食事摂取基準(2015 年版)の概要」リンの食事摂取基準(mg/日):https://www.mhlw.go.jp/file/04-Houdouhappyou-10904750-Kenkoukyoku-Gantaisakukenkouzoushinka/0000041955.pdf
理科ねっとわーく:https://rika-net.com/contents/cp0490b/contents/cheindex1.html
山﨑 友紀
最新記事 by 山﨑 友紀 (全て見る)
- 実験講座 番外編 アメリカ、サンフランシスコ湾での天然塩づくり - 2024年3月25日
- 実験講座 番外編 アメリカ カリフォルニアで見た多様な鳥たち - 2024年1月29日
- 実験講座 番外編 アメリカCalifornia Academy of Science(科学博物館)訪問 - 2023年11月27日